Модерен PRP: „Клиничен PRP“
През последните 10 години лечебната схема на PRP претърпя големи промени.Чрез експериментални и клинични изследвания сега имаме по-добро разбиране за физиологията на тромбоцитите и други клетки.В допълнение, няколко висококачествени систематични оценки, мета-анализи и рандомизирани контролирани проучвания показаха ефективността на PRP биотехнологията в много медицински области, включително дерматология, кардиохирургия, пластична хирургия, ортопедична хирургия, управление на болката, гръбначни заболявания и спортна медицина .
Текущата характеристика на PRP е неговата абсолютна концентрация на тромбоцити, която се променя от първоначалната дефиниция на PRP (включително концентрация на тромбоцити, по-висока от изходната стойност) до повече от 1 × 10 6/µL или около 5 пъти минималната концентрация на тромбоцити в тромбоцитите от базова линия.В обширния преглед на Fadadu et al.Бяха оценени 33 PRP системи и протоколи.Броят на тромбоцитите в крайния PRP препарат, произведен от някои от тези системи, е по-нисък от този на цялата кръв.Те съобщават, че тромбоцитният фактор на PRP се е повишил до 0,52 с комплекта за едно центрофугиране (Selphyl®).За разлика от това, EmCyte Genesis PurePRPII ® с двойно завъртане Концентрацията на тромбоцитите, произведена от устройството, е най-високата (1,6 × 10 6 /µL) .
Очевидно in vitro и животинските методи не са идеалната изследователска среда за успешна трансформация в клинична практика.По същия начин проучването за сравнение на устройствата не подкрепя решението, тъй като те показват, че концентрацията на тромбоцитите между PRP устройствата е много различна.За щастие, чрез технология и анализ, базирани на протеомика, можем да подобрим нашето разбиране за клетъчните функции в PRP, които влияят върху резултатите от лечението.Преди да се постигне консенсус относно стандартизираните PRP препарати и формулировки, PRP трябва да следва клиничните PRP формулировки, за да насърчи съществени механизми за възстановяване на тъканите и прогресивни клинични резултати.
Клинична PRP формула
Понастоящем ефективният клиничен PRP (C-PRP) се характеризира като сложен състав от автоложни многоклетъчни компоненти в малък обем плазма, получена от част от периферна кръв след центрофугиране.След центрофугиране, PRP и неговите нетромбоцитни клетъчни компоненти могат да бъдат възстановени от устройството за концентриране според различните клетъчни плътности (от които тромбоцитната плътност е най-ниска).
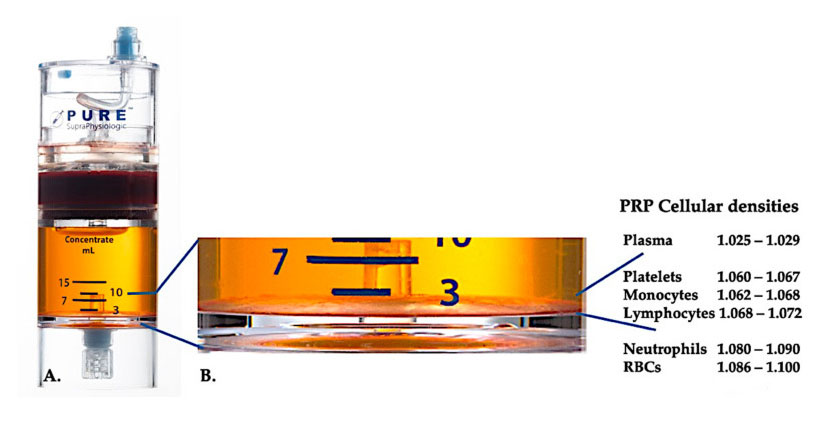
Използвайте PurePRP-SP ® Оборудване за разделяне на клетъчна плътност (EmCyte Corporation, Форт Майерс, Флорида, САЩ) беше използвано за цяла кръв след две процедури на центрофугиране.След първия процес на центрофугиране целият кръвен компонент беше разделен на два основни слоя, суспензия от тромбоцитна (бедна) плазма и слой червени кръвни клетки.В А втората стъпка на центрофугиране е завършена.Действителният PRP обем може да бъде извлечен за приложение от пациента.Увеличението в B показва, че има организиран многокомпонентен кафяв слой за утаяване на еритроцити (представен със синя линия) в долната част на оборудването, който съдържа високи концентрации на тромбоцити, моноцити и лимфоцити, въз основа на градиента на плътност.В този пример, съгласно протокола за подготовка на C-PRP с лоши неутрофили, ще бъдат извлечени минималният процент неутрофили (<0,3%) и еритроцити (<0,1%).
Тромбоцитна гранула
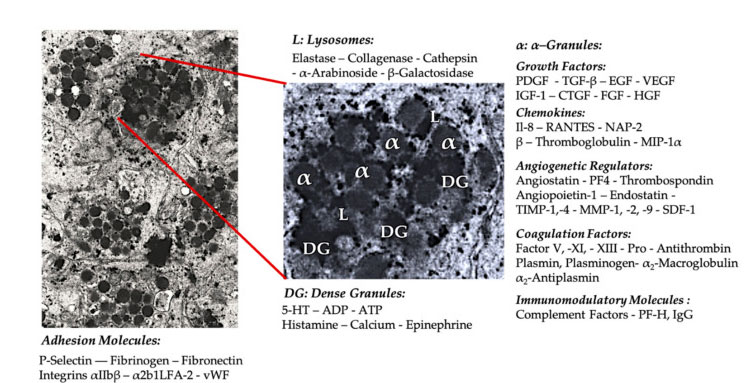
В ранното клинично приложение на PRP α-гранулите са най-често цитираната вътрешна структура на тромбоцитите, тъй като съдържат коагулационни фактори, голям брой PDGF и ангиогенни регулатори, но имат малка тромбогенна функция.Други фактори включват по-малко известни хемокинови и цитокинови компоненти, като тромбоцитен фактор 4 (PF4), предтромбоцитен основен протеин, Р-селектин (активатор на интегрин) и хемокин RANTES (регулиран чрез активиране, експресиращ нормални Т клетки и вероятно секретиращ).Цялостната функция на тези специфични компоненти на тромбоцитните гранули е да набират и активират други имунни клетки или да индуцират възпаление на ендотелните клетки.
Плътни гранулирани компоненти като ADP, серотонин, полифосфат, хистамин и адреналин се използват по-имплицитно като регулатори на активирането на тромбоцитите и тромбозата.Най-важното е, че много от тези елементи имат функцията да модифицират имунните клетки.Тромбоцитният ADP се разпознава от P2Y12ADP рецептора върху дендритни клетки (DC), като по този начин увеличава антигенната ендоцитоза.DC (антиген представяща клетка) е много важен за иницииране на Т-клетъчен имунен отговор и контролиране на защитния имунен отговор, който свързва вродената имунна система и адаптивната имунна система.В допълнение, тромбоцитният аденозин трифосфат (АТР) изпраща сигнали през Т клетъчния рецептор P2X7, което води до повишена диференциация на CD4 Т хелперни клетки в провъзпалителни Т хелперни 17 (Th17) клетки.Други компоненти на плътни гранули на тромбоцитите (като глутамат и серотонин) индуцират миграция на Т клетки и съответно увеличават диференциацията на моноцитите до DC.В PRP тези имуномодулатори, получени от плътни частици, са силно обогатени и имат значителни имунни функции.
Броят на преките и индиректните потенциални взаимодействия между тромбоцитите и други (рецепторни) клетки е голям.Следователно, прилагането на PRP в локалната патологична тъканна среда може да предизвика различни възпалителни ефекти.
Концентрация на тромбоцитите
C-PRP трябва да съдържа клинични дози от концентрирани тромбоцити, за да предизвика благоприятни терапевтични ефекти.Тромбоцитите в C-PRP трябва да стимулират клетъчната пролиферация, синтеза на мезенхимни и невротрофични фактори, да насърчават миграцията на хемотаксични клетки и да стимулират имунорегулаторната активност, както е показано на фигурата.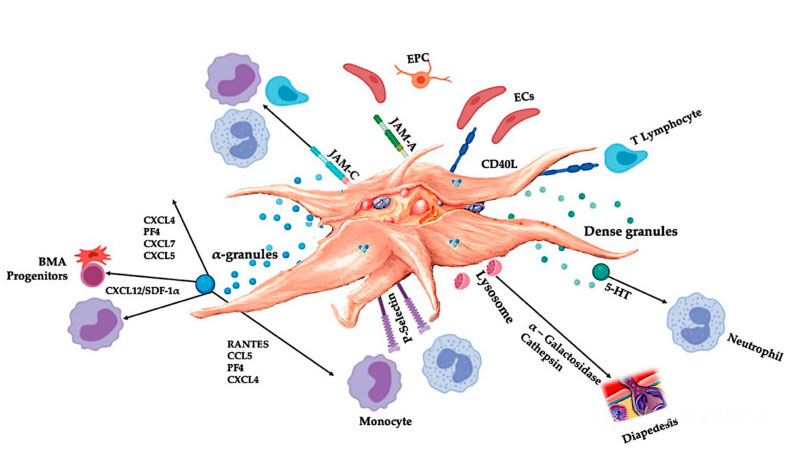
Активираните тромбоцити, освобождаването на PGF и адхезионните молекули медиират различни клетъчни взаимодействия: хемотаксис, клетъчна адхезия, миграция и клетъчна диференциация и регулират имунните регулаторни дейности.Тези взаимодействия между тромбоцитните клетки допринасят за ангиогенезата и възпалителната активност и в крайна сметка стимулират процеса на възстановяване на тъканите.Съкращения: BMA: аспират от костен мозък, EPC: ендотелни прогениторни клетки, EC: ендотелни клетки, 5-HT: 5-хидрокситриптамин, RANTES: активирана регулация на нормална Т-клетъчна експресия и предполагаема секреция, JAM: тип молекула на адхезионна връзка, CD40L: клъстер 40 лиганд, SDF-1 α: фактор-1 α, получен от стромални клетки, CXCL: хемокин (CXC мотив) лиганд, PF4: тромбоцитен фактор 4. Адаптирано от Everts et al.
Маркс е първият човек, който доказва, че заздравяването на костите и меките тъкани е подобрено и минималният брой на тромбоцитите е 1 × 10 6 /µL。 Тези резултати са потвърдени в изследване на лумбална фузия през междупрешленния отвор, когато дозата на тромбоцитите е по-голяма от 1,3 × При 106 тромбоцити/µL това изследване демонстрира повече сливане.В допълнение Giusti et al.Разкрит 1,5 × Механизмът за възстановяване на тъканите при доза от 109 изисква тромбоцити/mL за индуциране на функционална ангиогенеза чрез активността на ендотелните клетки.В последното проучване по-високите концентрации намаляват ангиогенезния потенциал на тромбоцитите в и около фоликулите.В допълнение, по-ранни данни показват, че дозата PRP също ще повлияе на резултатите от лечението.Следователно, за да се индуцира значително реакция на ангиогенеза и да се стимулира клетъчната пролиферация и клетъчната миграция, C-PRP трябва да съдържа най-малко 7,5 в 5-mL PRP бутилка за лечение × 10 9 може да достави тромбоцити.
В допълнение към зависимостта от дозата, ефектът на PRP върху клетъчната активност изглежда силно зависим от времето.Софи и др.Тези резултати предполагат, че краткосрочното излагане на човешки тромбоцитни лизати може да стимулира пролиферацията на костните клетки и хемотаксиса.Напротив, дългосрочното излагане на PRP ще доведе до по-ниски нива на алкална фосфатаза и образуване на минерали.
червена кръвна клетка
Червените кръвни клетки са отговорни за транспортирането на кислород до тъканите и преноса на въглероден диоксид от тъканите към белите дробове.Те нямат ядро и са съставени от хем молекули, които се свързват с протеини.Компонентите желязо и хем в червените кръвни клетки насърчават комбинацията от кислород и въглероден диоксид.Обикновено жизненият цикъл на червените кръвни клетки е около 120 дни.Те се отстраняват от кръвообращението от макрофаги чрез процес, наречен стареене на червените кръвни клетки.Червените кръвни клетки в PRP пробите могат да бъдат увредени при условия на срязване (например операция за кървене на цяла кръв, имуномедииран процес, оксидативен стрес или неадекватна схема на концентрация на PRP).Следователно клетъчната мембрана на червените кръвни клетки се разлага и освобождава токсичен хемоглобин (Hb), измерен чрез плазмен свободен хемоглобин (PFH), хем и желязо.].PFH и неговите продукти на разграждане (хем и желязо) водят заедно до вредни и цитотоксични ефекти върху тъканите, което води до оксидативен стрес, загуба на азотен оксид, активиране на възпалителни пътища и имуносупресия.Тези ефекти в крайна сметка ще доведат до дисфункция на микроциркулацията, локална вазоконстрикция и съдово увреждане, както и сериозно увреждане на тъканите.
Най-важното е, че когато червените кръвни клетки, съдържащи C-PRP, бъдат доставени в тъканта, това ще предизвика локална реакция, наречена ериптоза, която ще задейства освобождаването на ефективен инхибитор на миграцията на цитокини и макрофаги.Този цитокин инхибира миграцията на моноцити и макрофаги.Той упражнява силни провъзпалителни сигнали към околните тъкани, инхибира миграцията на стволови клетки и пролиферацията на фибробласти и води до значителна локална клетъчна дисфункция.Следователно е важно да се ограничи замърсяването на еритроцитите в PRP препаратите.В допълнение, ролята на червените кръвни клетки в регенерацията на тъканите никога не е била определена.Адекватното C-PRP центрофугиране и процес на подготовка обикновено намаляват или дори елиминират наличието на червени кръвни клетки, като по този начин се избягват неблагоприятните последици от хемолизата и полицитемията.
Левкоцити в C-PRP
Наличието на бели кръвни клетки в PRP препаратите зависи от лечебното оборудване и схемата на подготовка.В базираното на плазма PRP оборудване, белите кръвни клетки са напълно елиминирани;Въпреки това, белите кръвни клетки са значително концентрирани в PRP препарата на кафявия слой от утаяване на еритроцитите.Благодарение на своите имунни и защитни механизми на гостоприемника, белите кръвни клетки влияят значително върху вътрешната биология на острите и хроничните тъканни състояния.Тези функции ще бъдат разгледани по-долу.Следователно наличието на специфични левкоцити в C-PRP може да причини значителни клетъчни и тъканни ефекти.По-конкретно, различните PRP еритроцитни седиментационни кафяво-жълти слоеве системи използват различни схеми на приготвяне, като по този начин произвеждат различна пропорция на неутрофили, лимфоцити и моноцити в PRP.Еозинофилите и базофилите не могат да бъдат измерени в PRP препарати, тъй като техните клетъчни мембрани са твърде крехки, за да издържат на центробежните обработващи сили.
Неутрофили
Неутрофилите са основни левкоцити в много лечебни пътища.Тези пътища се комбинират с антимикробни протеини, присъстващи в тромбоцитите, за да образуват плътна бариера срещу инвазивни патогени.Наличието на неутрофили се определя според целта на лечението на C-PRP.Може да са необходими повишени нива на тъканно възпаление при PRP биотерапия за лечение на хронични рани или при приложения, насочени към растеж или заздравяване на костите.Важно е, че допълнителни неутрофилни функции са открити в няколко модела, подчертавайки тяхната роля в ангиогенезата и възстановяването на тъканите.Въпреки това, неутрофилите също могат да причинят вредни ефекти, така че не са подходящи за някои приложения.Zhou и Wang доказват, че използването на PRP, богат на неутрофили, може да доведе до увеличаване на съотношението на колаген тип III към колаген тип I, като по този начин влошава фиброзата и намалява здравината на сухожилията.Други вредни характеристики, медиирани от неутрофили, са освобождаването на възпалителни цитокини и матрични металопротеинази (ММР), които могат да стимулират възпаление и катаболизъм, когато се прилагат върху тъканите.
Левкомоноцит
В C-PRP мононуклеарните Т и В лимфоцити са по-концентрирани от всички други бели кръвни клетки.Те са тясно свързани с клетъчно-медиирания цитотоксичен адаптивен имунитет.Лимфоцитите могат да предизвикат клетъчни реакции за борба с инфекцията и адаптиране към нашественици.В допълнение, получените от Т-лимфоцитите цитокини (интерферон-γ [IFN-γ] и интерлевкин-4 (IL-4) засилват поляризацията на макрофагите. Verassar et al. Доказано е, че конвенционалните Т-лимфоцити могат индиректно да стимулират заздравяването на тъканите в миши модел чрез регулиране на диференциацията на моноцити и макрофаги.
Моноцит – мултипотентна възстановителна клетка
В зависимост от използваното устройство за подготовка на PRP, моноцитите може да изпъкнат или да не съществуват в бутилката за лечение с PRP.За съжаление тяхната производителност и способност за регенерация рядко се обсъждат в литературата.Поради това се обръща малко внимание на моноцитите в метода на приготвяне или крайната формула.Моноцитната група е хетерогенна, произхождаща от прогениторни клетки в костния мозък и транспортирана до периферните тъкани чрез пътя на хемопоетичните стволови клетки според стимулацията на микросредата.По време на хомеостаза и възпаление, циркулиращите моноцити напускат кръвния поток и се набират към наранени или разградени тъкани.Те могат да действат като макрофаги (M Φ) ефекторни клетки или прогениторни клетки.Моноцитите, макрофагите и дендритните клетки представляват мононуклеарната фагоцитна система (MPS). Типична характеристика на MPS е пластичността на неговия модел на генна експресия и функционалното припокриване между тези типове клетки.В дегенерирани тъкани, резидентни макрофаги, локално действащи растежни фактори, провъзпалителни цитокини, апоптотични или некротични клетки и микробни продукти инициират моноцитите да се диференцират в MPS клетъчни групи.Да предположим, че когато C-PRP, съдържащ моноцити с висок добив, се инжектира в локалната микросреда на заболяването, има вероятност моноцитите да се диференцират в M Φ, за да причинят големи клетъчни промени.
От моноцит до M Φ В процеса на трансформация, специфичен M Φ фенотип.През последните десет години е разработен модел, който интегрира M Φ. Сложният механизъм на активиране се описва като поляризация на две противоположни състояния: M Φ фенотип 1 (M Φ 1, класическо активиране) и M Φ фенотип 2 (M Φ 2, алтернативно активиране).M Φ 1 се характеризира с възпалителна секреция на цитокини (IFN-γ) и азотен оксид за създаване на ефективен механизъм за убиване на патогени.M Φ Фенотипът също произвежда васкуларен ендотелен растежен фактор (VEGF) и фибробластен растежен фактор (FGF).M Φ Фенотипът се състои от противовъзпалителни клетки с висока фагоцитоза.M Φ 2 Произвежда компоненти на извънклетъчния матрикс, ангиогенеза и хемокини и интерлевкин 10 (IL-10).В допълнение към защитата на патогените, M Φ може също да намали възпалението и да насърчи възстановяването на тъканите.Трябва да се отбележи, че M Φ 2 е подразделен на M in vitro Φ 2a、M Φ 2b и M Φ 2. Зависи от стимула.In vivo преводът на тези подтипове е труден, тъй като тъканта може да съдържа смесени M Φ групи.Интересно е, че въз основа на местни сигнали от околната среда и нива на IL-4, провъзпалителният M Φ 1 може да бъде преобразуван, за да насърчи възстановяването M Φ 2。 От тези данни е разумно да се предположи, че има високи концентрации на моноцити и M Φ C-PRP препарати могат да допринесат за по-добро възстановяване на тъканите, защото имат противовъзпалително възстановяване на тъкани и способности за трансдукция на клетъчен сигнал.
Объркана дефиниция на фракцията на белите кръвни клетки в PRP
Наличието на бели кръвни клетки в бутилките за лечение с PRP зависи от устройството за приготвяне на PRP и може да има значителни разлики.Има много спорове относно съществуването на левкоцитите и техния принос към различни суб-PRP продукти (като PRGF, P-PRP, LP-PRP, LR-PRP, P-PRF и L-PRF) В скорошен преглед шест рандомизирани контролирани проучвания (ниво на доказателства 1) и три проспективни сравнителни проучвания (ниво на доказателства 2) включват 1055 пациенти, което показва, че LR-PRP и LP-PRP имат сходна безопасност.Авторът заключава, че нежеланата реакция на PRP може да не е пряко свързана с концентрацията на белите кръвни клетки.В друго проучване LR-PRP не променя възпалителния интерлевкин (IL-1) при ОА коляно β、 IL-6, IL-8 и IL-17).Тези резултати подкрепят мнението, че ролята на левкоцитите в биологичната активност на PRP in vivo може да идва от кръстосаното взаимодействие между тромбоцитите и левкоцитите.Това взаимодействие може да стимулира биосинтезата на други фактори (като липоксиген), които могат да компенсират или насърчат регресията на възпалението.След първоначалното освобождаване на възпалителни молекули (арахидонова киселина, левкотриен и простагландин), липоксиген А4 се освобождава от активираните тромбоцити, за да предотврати активирането на неутрофилите.Именно в тази среда фенотипът M Φ от M Φ 1 преминава към M Φ 2。 В допълнение, има все повече доказателства, че циркулиращите мононуклеарни клетки могат да се диференцират в различни нефагоцитни клетъчни типове поради тяхната плурипотентност.
Типът PRP ще повлияе на MSC културата.В сравнение с чист PRP или PPP проби, LR-PRP може да индуцира значително по-висока пролиферация на MSCs, получени от костен мозък (BMMSCs), с по-бързо освобождаване и по-добра PGF биологична активност.Всички тези характеристики са благоприятни за добавяне на моноцити в бутилката за лечение с PRP и разпознаване на тяхната имуномодулираща способност и потенциал за диференциация.
Вродена и адаптивна имунна регулация на PRP
Най-известната физиологична функция на тромбоцитите е да контролират кървенето.Те се натрупват в мястото на увреждане на тъканите и увредените кръвоносни съдове.Тези събития са причинени от експресията на интегрини и селектини, които стимулират адхезията и агрегацията на тромбоцитите.Увреденият ендотел допълнително утежнява този процес, а откритият колаген и други протеини на субендотелната матрица насърчават дълбокото активиране на тромбоцитите.В тези случаи е доказана важната роля на взаимодействието между фактора на von Willebrand (vWF) и гликопротеина (GP), особено GP-Ib.След активиране на тромбоцитите, тромбоцитните α-、 плътни, лизозомни и Т-гранули регулират екзоцитозата и освобождават съдържанието си в извънклетъчната среда.
Адхезионна молекула на тромбоцитите
За да разберем по-добре ролята на PRP във възпалителните тъкани и тромбоцитите в имунния отговор, трябва да разберем как различните повърхностни рецептори на тромбоцитите (интегрини) и адхезионните молекули на свързване (JAM) и клетъчните взаимодействия могат да инициират критични процеси във вродения и адаптивен имунитет.
Интегрините са адхезионни молекули на клетъчната повърхност, открити в различни типове клетки и експресирани в големи количества върху тромбоцитите.Интегрините включват a5b1, a6b1, a2b1 LFA-2, (GPIa/IIa) и aIIbb3 (GPIIb/IIIa).Обикновено те съществуват в статично състояние с нисък афинитет.След активиране те преминават към състояние на висок афинитет на свързване на лиганда.Интегрините имат различни функции върху тромбоцитите и участват във взаимодействието на тромбоцитите с няколко вида бели кръвни клетки, ендотелни клетки и екстрацелуларен матрикс.В допълнение, комплексът GP-Ib-V-IX се експресира върху тромбоцитната мембрана и е основният рецептор за свързване с von vWF.Това взаимодействие медиира първоначалния контакт между тромбоцитите и откритите субендотелни структури.Тромбоцитният интегрин и GP комплексът са свързани с различни възпалителни процеси и играят важна роля в образуването на тромбоцитно-левкоцитния комплекс.По-конкретно, интегрин aIIbb3 е необходим за образуване на стабилен комплекс чрез комбиниране на фибриноген с рецептор на макрофаг 1 антиген (Mac-1) върху неутрофили.
Тромбоцитите, неутрофилите и съдовите ендотелни клетки експресират специфични клетъчни адхезионни молекули, наречени селектин.При възпалителни състояния тромбоцитите експресират Р-селектин и неутрофилен L-селектин.След активиране на тромбоцитите P-селектинът може да се свърже с лиганда PSGL-1, който съществува върху неутрофилите и моноцитите.В допълнение, свързването на PSGL-1 инициира вътреклетъчна сигнална каскадна реакция, която активира неутрофили чрез неутрофилен интегрин Mac-1 и свързан с функцията на лимфоцитите антиген 1 (LFA-1).Активираният Mac-1 се свързва с GPIb или GPIIb/IIIa върху тромбоцитите чрез фибриноген, като по този начин стабилизира взаимодействието между неутрофилите и тромбоцитите.В допълнение, активираният LFA-1 може да се комбинира с тромбоцитна междуклетъчна адхезионна молекула 2 за по-нататъшно стабилизиране на комплекса неутрофил-тромбоцит за насърчаване на дълготрайна адхезия с клетките.
Тромбоцитите и левкоцитите играят ключова роля във вродените и адаптивни имунни отговори
Тялото може да разпознае чужди тела и наранени тъкани при остри или хронични заболявания, за да инициира каскадна реакция на заздравяване на рани и възпалителен път.Вродената и адаптивна имунна система предпазва гостоприемника от инфекция, а белите кръвни клетки играят важна роля в припокриването между двете системи.По-конкретно, моноцитите, макрофагите, неутрофилите и естествените клетки убийци играят ключова роля във вродената система, докато лимфоцитите и техните подгрупи играят подобна роля в адаптивната имунна система.
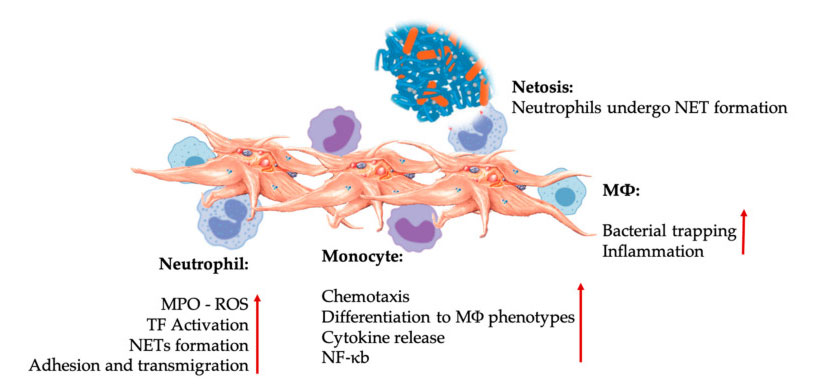
Взаимодействия на тромбоцити и левкоцити при взаимодействия на вродени имунни клетки.Тромбоцитите взаимодействат с неутрофили и моноцити и накрая с M Φ Взаимодействат, коригират и увеличават техните ефекторни функции.Тези тромбоцитно-левкоцитни взаимодействия водят до възпаление чрез различни механизми, включително NETosis.Съкращения: MPO: миелопероксидаза, ROS: реактивни кислородни видове, TF: тъканен фактор, NET: неутрофилен извънклетъчен капан, NF- κ B: ядрен фактор kappa B, M Φ: Макрофаги.
Вродена имунна система
Ролята на вродената имунна система е неспецифично да идентифицира инвазивни микроорганизми или тъканни фрагменти и да стимулира тяхното изчистване.Когато определени молекулярни структури, наречени рецептори за разпознаване на модели на повърхностна експресия (PRRs), се комбинират с молекулярни модели, свързани с патогени, и молекулярни модели, свързани с увреждане, ще се активира вродената имунна система.Има много видове PRR, включително Toll-подобен рецептор (TLR) и RIG-1 подобен рецептор (RLR).Тези рецептори могат да активират основния транскрипционен фактор kappa B (NF-κ B). Той също така регулира множество аспекти на вродения и адаптивен имунен отговор.Интересно е, че тромбоцитите също експресират различни имунорегулаторни рецепторни молекули на тяхната повърхност и цитоплазма, като Р-селектин, трансмембранен протеин CD40 лиганд (CD40L), цитокини (като IL-1 β, TGF- β) и специфичен за тромбоцитите TLR. Следователно, тромбоцитите могат да взаимодействат с различни имунни клетки.
Взаимодействие тромбоцити-бели клетки при вродения имунитет
Когато тромбоцитите навлязат или нахлуят в кръвния поток или тъкан, тромбоцитите са една от клетките, които първи откриват ендотелно увреждане и микробни патогени.Тромбоцитна агрегация и насърчаване на освобождаването на тромбоцитни агонисти ADP, тромбин и vWF, което води до тромбоцитно активиране и експресия на тромбоцитни хемокинови рецептори C, CC, CXC и CX3C, като по този начин причинява тромбоцити в заразеното място или нараняване.
Вродената имунна система е генетично предопределена да открива нашественици, като вируси, бактерии, паразити и токсини, или тъканни рани и рани.Това е неспецифична система, тъй като всеки патоген ще бъде идентифициран като чужд или несобствен и бързо локализиран.Вродената имунна система разчита на набор от протеини и фагоцити, които разпознават добре запазените характеристики на патогените и бързо активират имунния отговор, за да помогнат за елиминирането на нашествениците, дори ако гостоприемникът никога преди не е бил изложен на специфични патогени.
Неутрофилите, моноцитите и дендритните клетки са най-честите вродени имунни клетки в кръвта.Тяхното набиране е необходимо за адекватен ранен имунен отговор.Когато PRP се използва в регенеративната медицина, взаимодействието между тромбоцитите и белите клетки регулира възпалението, заздравяването на рани и възстановяването на тъканите.TLR-4 върху тромбоцитите стимулира взаимодействието между тромбоцитите и неутрофилите, което регулира така наречения оксидативен взрив на левкоцитите чрез регулиране на освобождаването на реактивни кислородни видове (ROS) и миелопероксидаза (MPO) от неутрофилите.В допълнение, взаимодействието между тромбоцит-неутрофил и неутрофилна дегранулация води до образуването на неутрофилно-екстрацелуларни капани (NETs).NET са съставени от неутрофилно ядро и друго неутрофилно вътреклетъчно съдържание, което може да улови бактерии и да ги убие чрез NETosis.Образуването на NET е основен механизъм за убиване на неутрофилите.
След активиране на тромбоцитите, моноцитите могат да мигрират към болни и дегенеративни тъкани, където извършват адхезионни дейности и секретират възпалителни молекули, които могат да променят хемотаксиса и протеолитичните свойства.В допълнение, тромбоцитите могат да индуцират моноцитно NF-κ B активиране за регулиране на ефекторната функция на моноцитите, което е ключовият медиатор на възпалителния отговор и активирането и диференциацията на имунните клетки.Тромбоцитите допълнително насърчават ендогенния оксидативен изблик на моноцити за насърчаване на унищожаването на фагоцитни патогени.Освобождаването на MPO се медиира от директното взаимодействие между тромбоцит-моноцит CD40L-MAC-1.Интересно е, че когато P-селектинът активира тромбоцитите при остри и хронични възпалителни тъканни състояния, получените от тромбоцитите хемокини PF4, RANTES, IL-1 β и CXCL-12 могат да предотвратят спонтанната апоптоза на моноцитите, но насърчават тяхната диференциация в макрофаги.
Адаптивна имунна система
След като неспецифичната вродена имунна система разпознае микробното или тъканното увреждане, специфичната адаптивна имунна система ще поеме.Адаптивните системи включват антиген-свързващи В-лимфоцити (В-клетки) и конвенционални Т-лимфоцити (Treg), които координират изчистването на патогените.Т клетките могат грубо да се разделят на помощни Т клетки (Th клетки) и цитотоксични Т клетки (Тс клетки, известни също като Т клетки убийци).Th клетките се разделят допълнително на Th1, Th2 и Th17 клетки, които имат ключови функции при възпаление.Th клетките могат да отделят провъзпалителни цитокини (напр. IFN-γ、 TNF- β) и няколко интерлевкина (напр. IL-17). Те са особено ефективни при предотвратяване на вътреклетъчни вирусни и бактериални инфекции. Th клетките стимулират пролиферацията и диференциацията на клетките, участващи в имунен отговор Тс клетките са ефекторни клетки, които могат да елиминират целевите вътреклетъчни и извънклетъчни микроорганизми и клетки.
Интересното е, че Th2 клетките произвеждат IL-4 и влияят на M Φ поляризацията, M Φ насочената регенерация M Φ 2 фенотип, докато IFN- γ M Φ се променят на възпалителен M Φ 1 фенотип, което зависи от дозата и времето на цитокините.След като IL-4 се активира, M Φ 2 индуцира Treg клетките да се диференцират в Th2 клетки и след това произвежда допълнителен IL-4 (положителна обратна връзка).Th клетките преобразуват M Φ Фенотипът е насочен към регенеративния фенотип в отговор на биологични агенти от тъканен произход.Този механизъм се основава на доказателствата, че Th клетките играят значителна роля в контролирането на възпалението и възстановяването на тъканите.
Взаимодействие тромбоцити-бели клетки в адаптивния имунитет
Адаптивната имунна система използва антиген-специфични рецептори и запомня срещани преди това патогени и ги унищожава, когато впоследствие срещне гостоприемника.Тези адаптивни имунни отговори обаче се развиват бавно.Кониас и др.Той показва, че тромбоцитният компонент допринася за възприемането на риска и възстановяването на тъканите и че взаимодействието между тромбоцитите и левкоцитите насърчава активирането на адаптивния имунен отговор.
По време на адаптивния имунен отговор, тромбоцитите насърчават моноцитните и макрофаговите отговори чрез съзряване на DC и NK клетки, което води до специфични Т-клетъчни и В-клетъчни отговори.Следователно компонентите на тромбоцитните гранули влияят директно върху адаптивния имунитет чрез експресиране на CD40L, молекула, която е от съществено значение за регулиране на адаптивния имунен отговор.Тромбоцитите чрез CD40L не само играят роля в представянето на антигена, но също така влияят на реакцията на Т клетките.Liu и др.Установено е, че тромбоцитите регулират CD4 Т клетъчния отговор по сложен начин.Тази диференцирана регулация на CD4 Т клетъчни подгрупи означава, че тромбоцитите насърчават CD4 Т клетките да реагират на възпалителни стимули, като по този начин произвеждат силни провъзпалителни и противовъзпалителни отговори.
Тромбоцитите също така регулират В-клетъчно медиираната адаптивна реакция към микробни патогени.Добре известно е, че CD40L върху активирани CD4 Т клетки ще задейства CD40 на В клетки, осигурявайки втория сигнал, необходим за зависимо от Т-клетките В лимфоцитно активиране, последващо преобразуване на алотипа и В клетъчна диференциация и пролиферация.Като цяло, резултатите ясно показват различните функции на тромбоцитите в адаптивния имунитет, което показва, че тромбоцитите свързват взаимодействието между Т-клетките и В-клетките чрез CD40-CD40L, като по този начин усилват Т-клетъчно-зависимия В-клетъчен отговор.В допълнение, тромбоцитите са богати на рецептори на клетъчната повърхност, които могат да насърчат активирането на тромбоцитите и да освободят голям брой възпалителни и биологично активни молекули, съхранявани в различни тромбоцитни частици, като по този начин повлияват вродения и адаптивен имунен отговор.
Разширена роля на серотонина, получен от тромбоцитите, в PRP
Серотонинът (5-хидрокситриптамин, 5-НТ) има ясна ключова роля в централната нервна система (ЦНС), включително толерантността към болка.Изчислено е, че по-голямата част от човешкия 5-HT се произвежда в стомашно-чревния тракт и след това чрез кръвообращението, където се абсорбира от тромбоцитите чрез транспортера за обратно поемане на серотонин и се съхранява в плътни частици при висока концентрация (65 mmol/L).5-НТ е добре известен невротрансмитер и хормон, който помага за регулирането на различни невропсихологични процеси в ЦНС (централен 5-НТ).Въпреки това, по-голямата част от 5-НТ съществува извън ЦНС (периферна 5-НТ) и участва в регулирането на системните и клетъчните биологични функции на множество органни системи, включително сърдечно-съдови, белодробни, стомашно-чревни, урогенитални и тромбоцитни функционални системи.5-HT има зависим от концентрацията метаболизъм върху различни видове клетки, включително адипоцити, епителни клетки и бели кръвни клетки.Периферният 5-HT също е мощен имунен модулатор, който може да стимулира или инхибира възпалението и да повлияе на различни имунни клетки чрез своя специфичен 5-HT рецептор (5HTR).
Паракринен и автокринен механизъм на ХТ
Активността на 5-HT се медиира от взаимодействието му с 5HTRs, което е суперсемейство със седем члена (5-HT 1 – 7) и най-малко 14 различни рецепторни подтипа, включително наскоро открития член 5-HT 7, неговите периферни и функция при управление на болката.В процеса на дегранулация на тромбоцитите, активираните тромбоцити секретират голям брой 5-HT, получен от тромбоцитите, който може да насърчи съдовата контракция и да стимулира активирането на съседни тромбоцити и лимфоцити чрез експресията на 5-HTR върху ендотелни клетки, гладкомускулни клетки и имунни клетки.Пакала и др.Изследван е митотичният ефект на 5-HT върху васкуларните ендотелни клетки и е определен потенциалът за насърчаване на растежа на увредени кръвоносни съдове чрез стимулиране на ангиогенезата.Как се регулират тези процеси не е напълно ясно, но може да включва диференциални двупосочни сигнални пътища в тъканната микросхема за регулиране на функциите на васкуларните ендотелни клетки и гладкомускулните клетки, фибробластите и имунните клетки чрез специфични 5-НТ рецептори върху тези клетки .Описана е автокринната функция на тромбоцитния 5-НТ след активиране на тромбоцитите [REF].Освобождаването на 5-НТ засилва активирането на тромбоцитите и набирането на циркулиращи тромбоцити, което води до активиране на сигнални каскадни реакции и възходящи ефектори, поддържащи реактивността на тромбоцитите.
Имуномодулиращ 5-HT ефект
Все повече и повече доказателства показват, че серотонинът може да играе роля в различни 5HTR като имунен модулатор.Според 5HTR, експресиран в различни левкоцити, участващи във възпалителна реакция, полученият от тромбоцитите 5-НТ действа като имунен регулатор както във вродената, така и в адаптивната имунна система.5-HT може да стимулира пролиферацията на Treg и да регулира функциите на В клетките, естествените клетки убийци и неутрофилите чрез набиране на DC и моноцити към мястото на възпалението.Последните проучвания показват, че 5-НТ, получен от тромбоцити, може да регулира функцията на имунните клетки при специфични условия.Следователно, използвайки C-PRP, концентрацията на тромбоцитите е по-голяма от 1 × 10 6/µL, може значително да помогне за транспортирането на концентрацията на 5-НТ, получена от големи тромбоцити, до тъканта.В микросредата, характеризираща се с възпалителни компоненти, PRP може да взаимодейства с няколко имунни клетки, които играят ключова роля в тези патологии, което може да повлияе на клиничните резултати.
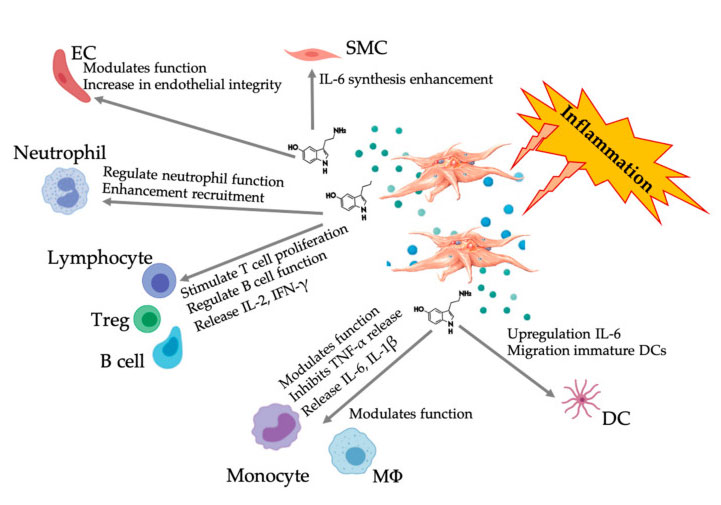
Фигура, показваща многостранния 5-HT отговор след активирането на възпалителни PRP тромбоцити.След активирането на тромбоцитите, тромбоцитите освобождават своите гранули, включително 5-НТ в плътни гранули, които имат широк спектър от диференциални ефекти върху различни имунни клетки, ендотелни клетки и гладкомускулни клетки.Съкращения: SMC: гладкомускулни клетки, EC: ендотелни клетки, Treg: конвенционални Т лимфоцити, M Φ: макрофаги, DC: дендритни клетки, IL: интерлевкин, IFN-γ: интерферон γ。 Модифицирано и адаптирано от Everts et al.и Hull et al.
Аналгетичен ефект на PRP
Активираните тромбоцити ще освободят много провъзпалителни и противовъзпалителни медиатори, които могат не само да причинят болка, но и да намалят възпалението и болката.Веднъж приложена, типичната динамика на тромбоцитите на PRP променя микросредата преди тъканното възстановяване и регенерация чрез различни сложни пътища, свързани с анаболизъм и катаболизъм, клетъчна пролиферация, диференциация и регулиране на стволови клетки.Тези характеристики на PRP водят до прилагането на PRP при различни клинични патологични състояния, обикновено свързани с хронична болка (като спортна травма, ортопедично заболяване, гръбначно заболяване и сложна хронична рана), въпреки че точният механизъм не е напълно определен.
През 2008 г. Evertz et al.Това е първото рандомизирано контролирано проучване, което отчита аналгетичния ефект на препарата PRP, който се приготвя от кафявия слой на автоложната скорост на утаяване на еритроцитите и се активира с автоложен тромбин след операция на рамото.Те отбелязаха значително намаляване на резултатите от визуалната аналогова скала, употребата на аналгетици на базата на опиоиди и по-успешна следоперативна рехабилитация.Трябва да се отбележи, че те отразяват аналгетичния ефект на активираните тромбоцити и спекулират върху механизма на тромбоцитите, освобождаващи 5-НТ.Накратко, тромбоцитите са латентни в прясно приготвен PRP.След активирането на тромбоцитите пряко или индиректно (тъканен фактор), тромбоцитите променят формата си и произвеждат достатъчно фалшиви, за да насърчат агрегацията на тромбоцитите.След това освобождават вътреклетъчни α- и плътни частици.Тъканта, третирана с активиран PRP, ще бъде нападната от PGF, цитокини и други тромбоцитни лизозоми.По-конкретно, когато плътните частици освободят съдържанието си, те ще освободят голямо количество 5-HT, което регулира болката.При C-PRP концентрацията на тромбоцитите е 5 до 7 пъти по-висока от тази в периферната кръв.Следователно освобождаването на 5-НТ от тромбоцитите е астрономическо.Интересното е, че Sprott et al.Докладът отбелязва, че болката е значително облекчена след акупунктура и моксибус, концентрацията на тромбоцитния 5-HT е значително намалена и след това плазменото ниво на 5-HT е повишено.
В периферните, тромбоцитите, мастоцитите и ендотелните клетки ще освободят ендогенен 5-НТ по време на тъканно увреждане или хирургична травма.Интересното е, че разнообразие от 5-НТ рецептори на неврони бяха открити в периферната област, което потвърди, че 5-НТ може да повлияе на ноцицептивното предаване в периферната област.Тези проучвания показват, че 5-НТ може да повлияе на ноцицептивното предаване на периферните тъкани чрез 5-НТ1, 5-НТ2, 5-НТ3, 5-НТ4 и 5-НТ7 рецептори.
Системата 5-HT представлява мощна система, която може да намали и увеличи степента на болка след вредна стимулация.Централната и периферната регулация на ноцицептивните сигнали и промените в 5-НТ системата са докладвани при пациенти с хронична болка.През последните години голям брой проучвания са фокусирани върху ролята на 5-HT и съответните му рецептори при обработката и регулирането на вредна информация, което води до лекарства като селективни инхибитори на обратното захващане на серотонина (SSRI).Това лекарство инхибира обратното поемане на серотонин в пресинаптичните неврони след освобождаването на серотонин.Той влияе върху продължителността и интензивността на комуникацията на серотонин и е алтернативно лечение на хронична болка.Необходими са по-нататъшни клинични изследвания, за да се разбере ясно молекулярният механизъм на PRP-производната 5-HT регулация на болката при хронични и дегенеративни заболявания.
Други данни за решаване на потенциалния аналгетичен ефект на PRP могат да бъдат получени след аналгетичния животински тест.Сравнителните статистически заключения в тези модели са трудни, тъй като тези проучвания съдържат твърде много променливи.Въпреки това, някои клинични проучвания са насочени към ноцицептивните и аналгетичните ефекти на PRP.Няколко проучвания показват, че пациентите, лекувани за тендиноза или разкъсвания на ротаторния маншет, имат слабо облекчаване на болката.За разлика от това, няколко други проучвания показват, че PRP може да намали или дори да премахне болката при пациенти с дегенерация на сухожилие, ОА, плантарен фасциит и други заболявания на краката и глезените.Крайната концентрация на тромбоцитите и биологичният клетъчен състав са идентифицирани като ключови характеристики на PRP, които помагат да се наблюдава постоянният аналгетичен ефект след прилагането на PRP.Други променливи включват метод на доставяне на PRP, технология на приложение, протокол за активиране на тромбоцитите, ниво на биологична активност на освободените PGF и цитокини, тип тъкан на приложение на PRP и тип нараняване.
Трябва да се отбележи, че Kuffler разрешава потенциала на PRP за облекчаване на болката при пациенти с лека до тежка хронична невропатична болка, вторична на увредения нерегенеративен нерв.Целта на това проучване е да се изследва дали невропатичната болка може да бъде намалена или отслабена поради PRP, насърчаващ регенерацията на аксоните и реинервацията на целевия нерв.Изненадващо, сред пациентите, получаващи лечение, невропатичната болка все още е елиминирана или облекчена най-малко шест години след операцията.В допълнение, всички пациенти започнаха да облекчават болката в рамките на три седмици след прилагането на PRP.
Напоследък подобни аналгетични PRP ефекти са наблюдавани в областта на постоперативните рани и грижата за кожата.Интересното е, че авторите съобщават за физиологичните аспекти на болката в раната, свързана със съдово увреждане и хипоксия на кожната тъкан.Те също така обсъдиха значението на ангиогенезата за оптимизиране на оксигенацията и доставката на хранителни вещества.Тяхното проучване показа, че в сравнение с контролната група, пациентите, получаващи PRP лечение, са имали по-малко болка и значително повишена ангиогенеза.И накрая, Johal и колегите му извършиха систематичен преглед и мета-анализ и заключиха, че PRP може да намали болката след използване на PRP при ортопедични показания, особено при пациенти, получаващи външен епикондилит и лечение на ОА на коляното.За съжаление, това проучване не уточнява ефектите на белите кръвни клетки, концентрацията на тромбоцитите или употребата на екзогенни тромбоцитни активатори, тъй като тези променливи биха повлияли на общата ефективност на PRP.Оптималната PRP концентрация на тромбоцитите за максимално облекчаване на болката не е ясна.В модела на тендиноза при плъх, концентрацията на тромбоцитите е 1,0 × 10 6 / μ При L болката може да бъде напълно облекчена, докато облекчаването на болката, причинено от PRP с половината от концентрацията на тромбоцитите, е значително намалено.Ето защо ние насърчаваме повече клинични проучвания за изследване на аналгетичните ефекти на различни PRP препарати.
PRP и ефект на ангиогенеза
C-PRP препаратите в прецизната регенеративна медицина позволяват доставяне на биомолекули, освободени от високи концентрации на тромбоцити, активирани в местата на целевата тъкан.Следователно са инициирани различни каскадни реакции, които допринасят за имунната регулация на място, възпалителния процес и ангиогенезата за насърчаване на заздравяването и възстановяването на тъканите.
Ангиогенезата е динамичен многоетапен процес, включващ покълване и тъканни микросъдове от вече съществуващи кръвоносни съдове.Ангиогенезата е напреднала благодарение на различни биологични механизми, включително миграция на ендотелни клетки, пролиферация, диференциация и делене.Тези клетъчни процеси са предпоставка за образуването на нови кръвоносни съдове.Те са от съществено значение за растежа на вече съществуващите кръвоносни съдове, за да възстановят притока на кръв и да поддържат високата метаболитна активност на тъканното възстановяване и регенерация.Тези нови кръвоносни съдове позволяват доставянето на кислород и хранителни вещества и отстраняването на страничните продукти от третираните тъкани.
Активността на ангиогенезата се регулира чрез стимулиране на ангиогенен фактор VEGF и антиангиогенни фактори (напр. ангиостатин и тромбоспондин-1 [TSP-1]).В болната и деградирала микросреда (включително ниско кислородно напрежение, ниско pH и високо ниво на млечна киселина), локалните ангиогенни фактори ще възстановят активността на ангиогенезата.
Няколко разтворими среди на тромбоцити, като основен FGF и TGF-β и VEGF могат да стимулират ендотелните клетки да произвеждат нови кръвоносни съдове.Landsdown и Fortier съобщават за различни резултати, свързани със състава на PRP, включително вътрешнотромбоцитните източници на много ангиогенни регулатори.Освен това те заключиха, че увеличаването на ангиогенезата допринася за заздравяването на заболяването MSK в области с лоша васкуларизация, като разкъсване на менискус, нараняване на сухожилие и други области с лоша васкуларизация.
Насърчаване и антиангиогенни тромбоцитни свойства
През последните няколко десетилетия публикувани проучвания доказват, че тромбоцитите играят ключова роля в първичната хемостаза, образуването на съсиреци, освобождаването на растежен фактор и цитокини и регулирането на ангиогенезата като част от процеса на възстановяване на тъканите.Парадоксално, PRP α- гранулите съдържат арсенал от проангиогенни растежни фактори, антиангиогенни протеини и цитокини (като PF4, инхибитор на плазминогенния активатор-1 и TSP-1) и са насочени към освобождаването на специфични фактори, които играят роля .Роля в ангиогенезата.Следователно, ролята на PRP в контролирането на регулацията на ангиогенезата може да се дефинира чрез активирането на специфични рецептори на клетъчната повърхност, TGF-β Иницииране на проангиогенни и антиангиогенни реакции.Способността на тромбоцитите да упражняват пътя на ангиогенезата е потвърдена при патологична ангиогенеза и туморна ангиогенеза.
Произведен от тромбоцитите ангиогенен растежен фактор и антиангиогенен растежен фактор, получен от α- И плътни и адхезивни молекули.Най-важното е, че общоприето е, че общият ефект на тромбоцитите върху ангиогенезата е проангиогенен и стимулиращ.Очаква се, че PRP терапията ще контролира индукцията на ангиогенеза, което ще допринесе за лечебния ефект на много заболявания, като заздравяване на рани и възстановяване на тъкани.Прилагането на PRP, по-специално прилагането на висока концентрация на PGF и други тромбоцитни цитокини, може да индуцира ангиогенеза, ангиогенеза и артериогенеза, тъй като фактор 1а, получен от стромални клетки, се свързва с CXCR4 рецептора върху ендотелните прогениторни клетки.Бил и др.Предполага се, че PRP увеличава исхемичната неоваскуларизация, което може да се дължи на стимулиране на ангиогенезата, ангиогенезата и артериогенезата.В техния in vitro модел пролиферацията на ендотелни клетки и образуването на капиляри се индуцират от голям брой различни PDG, от които VEGF е основният ангиогенен стимулатор.Друг важен и съществен фактор за възстановяване на пътя на ангиогенезата е синергията между множество PGF.Ричардсън и др.Доказано е, че синергичната активност на ангиогенния фактор тромбоцитен растежен фактор-bb (PDGF-BB) и VEGF води до бързо образуване на зряла съдова мрежа в сравнение с активността на индивидуалния растежен фактор.Комбинираният ефект на тези фактори наскоро беше потвърден в проучване за подобряване на церебралната колатерална циркулация при мишки с дългосрочна хипоперфузия.
Най-важното е, че in vitro проучване измерва пролиферативния ефект на човешки ендотелни клетки от пъпна вена и различни концентрации на тромбоцити при избора на устройство за подготовка на PRP и стратегия за дозиране на тромбоцитите и резултатите показват, че оптималната доза на тромбоцитите е 1,5 × 10 6 тромбоцити/μ 50. За насърчаване на ангиогенезата.Твърде високата концентрация на тромбоцитите може да инхибира процеса на ангиогенеза, така че ефектът е слаб.
Клетъчно стареене, стареене и PRP
Клетъчното стареене може да бъде предизвикано от различни стимули.Това е процес, при който клетките спират да се делят и претърпяват уникални фенотипни промени, за да се предотврати неограниченият растеж на увредените клетки, което играе важна роля в превенцията на рака.В процеса на физиологично стареене, стареенето на клетъчната репликация също ще насърчи стареенето на клетките и способността за регенерация на MSC ще бъде намалена.
Ефекти от стареенето и стареенето на клетките
In vivo, много видове клетки ще стареят и ще се натрупват в различни тъкани по време на стареенето, сред които има голям брой стареещи клетки.Натрупването на стареещи клетки изглежда се увеличава с напредване на възрастта, увреждане на имунната система, увреждане на тъканите или фактори, свързани със стреса.Механизмът на клетъчното стареене е идентифициран като патогенен фактор за заболявания, свързани с възрастта, като остеоартрит, остеопороза и дегенерация на междупрешленните дискове.Разнообразие от стимули ще влошат стареенето на клетките.В отговор свързаният със стареенето секреторен фенотип (SASP) ще секретира високи концентрации на протеинови клетки и цитокини.Този специален фенотип е свързан със стареещите клетки, в които те секретират високи нива на възпалителни цитокини (като IL-1, IL-6, IL-8), растежни фактори (като TGF-β, HGF, VEGF, PDGF), MMP и катепсин.В сравнение с младите хора, доказано е, че SAPS се увеличава с възрастта, тъй като процесът на стабилно състояние се разрушава, което води до стареене на клетките и намалена способност за регенерация.По-конкретно при ставни заболявания и заболявания на скелетната мускулатура.В това отношение, имунното стареене се счита за значителна промяна в спектъра на секреция на имунните клетки, което показва, че концентрацията на TNF-a, IL-6 и/или Il-1b се увеличава, което води до нискостепенно хронично възпаление.Струва си да се отбележи, че дисфункцията на стволовите клетки също е свързана с неклетъчни автономни механизми, като стареещи клетки, особено производството на провъзпалителни и антирегенеративни фактори чрез SASP.
Напротив, SASP може също така да стимулира клетъчната пластичност и препрограмирането на съседни клетки.В допълнение, SASP може да организира комуникацията с различни имунни медиатори и да активира имунните клетки, за да насърчи изчистването на стареещите клетки.Разбирането на ролята и функцията на стареещите клетки ще допринесе за заздравяването и тъканното ремоделиране на MSK мускулите и хроничните рани.
Трябва да се отбележи, че Ritcka et al.Проведено е обширно проучване и е открита основната и полезна роля на SASP за насърчаване на клетъчната пластичност и регенерация на тъканите и е въведена концепцията за преходно лечение на стареещите клетки.Те предпазливо споменаха, че стареенето е предимно полезен и регенеративен процес.
Стареене на клетките и потенциал на PRP
Тъй като броят на стволовите клетки намалява, стареенето ще повлияе на работата на стволовите клетки.По подобен начин при хората характеристиките на стволовите клетки (като сухота, пролиферация и диференциация) също намаляват с възрастта.Уанг и Нирмала съобщават, че стареенето ще намали характеристиките на стволовите клетки на сухожилията и броя на рецепторите на растежния фактор.Проучване върху животни показва, че концентрацията на PDGF при млади коне е висока.Те заключават, че увеличаването на броя на GF рецепторите и броя на GF при млади индивиди може да има по-добър клетъчен отговор на PRP лечение, отколкото по-възрастните индивиди при млади индивиди.Тези открития разкриват защо лечението с PRP може да бъде по-малко ефективно или дори неефективно при пациенти в напреднала възраст с по-малко стволови клетки и „лошо качество“.Доказано е, че процесът на стареене на стареещия хрущял се обръща и периодът на почивка на хондроцитите се увеличава след инжектиране на PRP.Jia и др.Използва се за изследване на миши дермални фибробласти in vitro фотостареене, със и без PRP лечение, за да се изясни механизмът на противодействие на PGF в този модел.PRP групата показва директен ефект върху извънклетъчния матрикс, увеличава колагена тип I и намалява синтеза на металопротеинази, което показва, че PRP може да противодейства на стареенето на клетките, а също и при дегенеративно MSK заболяване.
В друго проучване PRP е използван за събиране на стари стволови клетки от костен мозък от възрастни мишки.Установено е, че PRP може да възстанови различни функции на стволови клетки от стареенето, като клетъчна пролиферация и образуване на колонии, и да реконструира маркерите, свързани със стареенето на клетките.
Наскоро Oberlohr и колегите му обстойно проучиха ролята на клетъчното стареене при отслабването на мускулната регенерация и оцениха PRP и бедната на тромбоцити плазма (PPP) като биологични възможности за лечение за възстановяване на скелетните мускули.Те предвиждаха, че PRP или PPP лечението за възстановяване на скелетните мускули ще се основава на биологични фактори, персонализирани за SASP специфични клетъчни маркери и други фактори, които водят до развитие на фиброза.
Разумно е да се смята, че преди прилагането на PRP, целевото стареене на клетките може да подобри регенерационните характеристики на ефикасността на биологичното лечение чрез намаляване на местните SASP фактори.Предполага се, че друга възможност за подобряване на резултатите от лечението с PRP и PPP за регенерация на скелетната мускулатура е селективното отстраняване на стареещите клетки със стареещи чистачи.Няма съмнение, че последните резултати от изследванията за ефекта на PRP върху стареенето и стареенето на клетките са очарователни, но те все още са в начален етап.Следователно е неразумно да се правят каквито и да било предложения в момента.
(Съдържанието на тази статия е препечатано и ние не предоставяме никаква изрична или подразбираща се гаранция за точността, надеждността или пълнотата на съдържанието, съдържащо се в тази статия, и не носим отговорност за мненията в тази статия, моля, разберете.)
Време на публикуване: 01 март 2023 г